Κάθε φαινόμενο σχεδόν, συνοδεύεται από μεταβολή μορφών ενέργειας και από μεταφορά ποσοτήτων ενέργειας από ένα σύστημα σε άλλο. Επειδή δε η συνολική ενέργεια ούτε καταστρέφεται, ούτε δημιουργείται, είναι ανάγκη να μάθουμε να «τηρούμε τα λογιστικά» σε τέτοιες ενεργειακές μεταβολές.
Η θερμοχημεία μελετά τις μεταβολές της θερμότητας στις χημικές αντιδράσεις.
Ενέργεια
Σχετίζεται με την ικανότητα ενός συστήματος να παραγάγει έργο.
Μορφές Ενέργειας
- Θερμική ενέργεια
Σχετίζεται με την τυχαία κίνηση των μορίων και ατόμων - Χημική ενέργεια
Είναι η ενέργεια των δεσμών στις χημικές ενώσεις - Πυρηνική ενέργεια
Είναι η ενέργεια που απελευθερώνεται όταν μετασχηματίζονται ατομικοί πυρήνες. - Ηλεκτρική ενέργεια
Συνδέεται με την κίνηση των ηλεκτρονίων (ηλεκτρ. φορτία) - Δυναμική ενέργεια
Η ενέργεια που έχει ένα σώμα λόγω της θέσης του - Κινητική ενέργεια
Η ενέργεια που έχει ένα σώμα λόγω της ταχύτητας του
Θερμότητα είναι η ενέργεια που ανταλλάσσει το σύστημα με το περιβάλλον του λόγω διαφοράς θερμοκρασίας μεταξύ τους
Θερμοκρασία είναι το μέτρο της θερμικής ενέργειας ενός σώματος
Θερμοκρασία ≠ Θερμότητα
Μονάδες Θερμότητας
Joule (SI), kJ (1kJ = 1.000 J)
cal Είναι το ποσό θερμότητας που απαιτείται για να αυξηθεί η θερμοκρασία 1 g H2O κατά ένα βαθμό ( Από 14,5ο στους 15,5ο), kcal = 1.000 cal
1 cal = 4,184 J 1 kcal = 4,184 kJ
1 J = 0,24 cal 1 kJ = 0,24 kcal
Σύστημα και περιβάλλον
Όταν γίνεται μελέτη ενός φαινομένου από την πλευρά της ενέργειας γίνεται πάντα αναφορά σε ένα σύστημα, μέσα στο οποίο συμβαίνει το φαινόμενο και στο περιβάλλον.
Σύστημα ονομάζεται το υποσύνολο του σύμπαντος που επιθυμούμε να μελετήσουμε. Συνήθως στη χημεία ως σύστημα ορίζουμε ένα σύνολο ουσιών που υφίστανται μια χημική μεταβολή.
Περιβάλλον ονομάζεται όλο το υπόλοιπο σύμπαν εκτός του συστήματος.
Όριο ονομάζεται η διεπιφάνεια που διαχωρίζει το σύστημα από το περιβάλλον.
Ένα θερμοδυναμικό σύστημα μπορεί να είναι ανοικτό, κλειστό ή μονωμένο σε σχέση με το περιβάλλον.
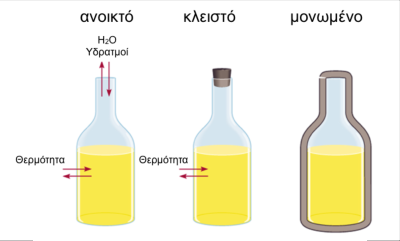
Ενθαλπία
Ένα σύστημα που περιέχει μία ή περισσότερες ουσίες έχει ενέργεια που ονομάζεται εσωτερική ενέργεια (U). Η εσωτερική ενέργεια είναι η ολική ενέργεια του συστήματος και περιλαμβάνει την κινητική ενέργεια των σωματιδίων του συστήματος (μορίων, ιόντων, ατόμων) και την δυναμική ενέργεια που οφείλεται στους χημικούς δεσμούς και στις διαμοριακές δυνάμεις.
Ενθαλπία ονομάζεται η ολική ενέργεια του συστήματος όταν αυτό βρίσκεται υπό σταθερή πίεση, και ορίζεται από την σχέση.
H = U + PV
Θερμοχημεία είναι ο κλάδος της χημείας που ασχολείται με τα ποσά θερμότητας που ανταλλάσσονται μεταξύ χημικού συστήματος και περιβάλλοντος κατά τη διάρκεια διεξαγωγής των χημικών φαινομένων. Όταν οι ανταλλαγές αυτές συντελούνται σε ένα χημικό σύστημα υπό σταθερή πίεση (πράγμα που είναι η συνήθης περίπτωση), τότε ταυτίζονται με τη μεταβολή ενθαλπίας του συστήματος.
Η θερμοδυναμική κατάσταση ενός συστήματος καθορίζεται με βάση τα καταστατικά μεγέθη που είναι:
- Η θερμοκρασία (Τ)
- Ο όγκος (V)
- Η πίεση (P)
- Η σύσταση, αριθμός mol (n)
Η ενθαλπία είναι μια καταστατική ιδιότητα του συστήματος, εξαρτάται δηλαδή από τα καταστατικά μεγέθη και όχι από την πορεία που έφτασε το σύστημα στην συγκεκριμένη κατάσταση.
Αν ένα σύστημα αποτελείται από τρεις ουσίες Α, Β, Γ, τότε η συνολική ενθαλπία του συστήματος είναι το άθροισμα των ενθαλπιών των συστατικών του συστήματος.
Ηολική = ΗΑ + ΗΒ + ΗΓ
Ενώ είναι σχεδόν αδύνατο να μετρήσουμε την ενθαλπία ενός συστήματος, μπορούμε να μετρήσουμε εύκολα τη μεταβολή ενθαλπίας.
ΔΗ = Ητελ. – Ηαρχ.
Μεταβολή ενθαλπίας σε μια αντίδραση
Η μεταβολή ενθαλπίας σε μια αντίδραση είναι η διαφορά μεταξύ της ενθαλπίας των προϊόντων και την ενθαλπίας των αντιδρόντων.
ΔΗ = Ηπροϊόντων – Ηαντιδρόντων
Την μεταβολή αυτή της ενθαλπίας μπορούμε να την μετρήσουμε γιατί είναι ίση με το ποσό θερμότητας (q) που εκλύεται ή απορροφάται από το σύστημα όταν η αντίδραση γίνεται υπό σταθερή πίεση.
 |
|
ΕΞΩΘΕΡΜΗ |
ΕΝΔΟΘΕΡΜΗ |
|
Εκλύεται ενέργεια q με μορφή θερμότητας προς το περιβάλλον |
Απορροφάται ενέργεια q με μορφή θερμότητας από το περιβάλλον |
|
Ηπρ. < Ηαντ. ή ΔΗ = Ηπρ – Ηαντ < 0 και q > 0 |
Ηπρ. > Ηαντ. ή ΔΗ = Ηπρ – Ηαντ > 0 και q < 0 |
-
Η ενθαλπία δεν είναι θερμότητα. Ένα σύστημα δίνει ή παίρνει ενέργεια με την μορφή της θερμότητας, οπότε υπάρχει και μεταβολή της ενθαλπίας του.
-
Η μεταβολή της ενθαλπίας ΔΗ αναφέρεται στο σύστημα, ενώ το ποσό θερμότητας (q) στο περιβάλλον. Έτσι στην εξώθερμη εκλύεται θερμότητα προς το περιβάλλον και ισχύει ΔΗ < 0 και q > 0, ενώ στην ενδόθερμη απορροφάται ενέργεια από το περιβάλλον και ισχύει ΔΗ > 0 και q < 0.
 |
ΔραστηριότηταΔείτε την συμπεριφορά εξώθερμης και ενδόθερμης αντίδρασης |
Θερμοχημικές Εξισώσεις
Είναι οι χημικές εξισώσεις που γράφεται και η μεταβολή της ενθαλπίας που παρατηρείται κατά την πραγματοποίηση της αντίδρασης.
CH4(g) + 2O2(g) → CO2(g) + 2H2O(l) ΔΗ = -890 kJ

Στις θερμοχημικές εξισώσεις αναγράφεται πάντα η φυσική κατάσταση των ουσιών.
(g): αέριο (gas)
(l): υγρό (liquid)
(s): στερεό (solid)
(aq): υδατικό διάλυμα (aqueous solution)
Ενθαλπία αντίδρασης – ΔΗ
Ενθαλπία αντίδρασης ορίζεται η μεταβολή ενθαλπίας AH μεταξύ των αντιδρώντων και προϊόντων, για δεδομένες συνθήκες πίεσης και θερμοκρασίας.
ΔH = Hπροϊόντων – Hαντιδρώντων
H μεταβολή της ενθαλπίας μιας αντίδρασης εξαρτάται:
1. Από τη φύση των αντιδρώντων
2. Από τη φυσική κατάσταση των αντιδρώντων και προϊόντων
3. Από τις συνθήκες πίεσης και θερμοκρασίας, κάτω από τις οποίες λαμβάνει χώρα η αντίδραση.
Πρότυπη ενθαλπία αντίδρασης, ΔΗ0
Σε πρότυπη κατάσταση, η αντίστοιχη μεταβολή της ενθαλπίας λέγεται πρότυπη μεταβολή ενθαλπίας ή πρότυπη ενθαλπία και συμβολίζεται με ΔΗ0
H πρότυπη κατάσταση μιας ουσίας (στοιχείου ή ένωσης) είναι η πιο σταθερή μορφή της σε
• θερμοκρασία 25 ο C και
• πίεση 1 atm
• συγκέντρωση c = 1 M (για διαλύματα)
Πρότυπη ενθαλπία σχηματισμού, ΔΗ0f (formation)
Πρότυπη ενθαλπία σχηματισμού μιας ένωσης, ΔHof, είναι η μεταβολή της ενθαλπίας κατά το σχηματισμό 1 mol της ένωσης από τα συστατικά της στοιχεία της, σε πρότυπη κατάσταση.
C(γραφίτης) + O2(g) → CO2(g) ΔΗ = -393,5 kJ
H ΔHof των στοιχείων στην πιο σταθερή μορφή τους θεωρείται μηδέν.
Επίσης η τιμή της ΔH0 μιας αντίδρασης μπορεί να υπολογιστεί με βάση τις πρότυπες ενθαλπίες σχηματισμού των ενώσεων που μετέχουν στην αντίδραση:
ΔΗ0 = ΣΔΗ0f πρ – ΣΔΗ0f αντ
Πρότυπη ενθαλπία καύσης, ΔΗ0c (combustion)
Πρότυπη ενθαλπία καύσης μιας ουσίας, Δ H°c , είναι η μεταβολή της ενθαλπίας κατά την πλήρη καύση 1 mol της ουσίας, σε πρότυπη κατάσταση.
Πρότυπη ενθαλπία εξουδετέρωσης, ΔHon (neutralization)
Πρότυπη ενθαλπία εξουδετέρωσης, ΔHon , είναι η μεταβολή της ενθαλπίας κατά την πλήρη εξουδετέρωση (σε αραιό υδατικό διάλυμα) 1 mol H+ ενός οξέος με μια βάση ή 1 mol OH– μιας βάσης με ένα οξύ, σε πρότυπη κατάσταση.
Κατά την εξουδετέρωση ισχυρού οξέος με ισχυρή βάση η τιμή της ΔΗ°n είναι περίπου σταθερή, ανεξάρτητα από το είδος του οξέος ή της βάσης που χρησιμοποιούμε.
ΔΗ°n= -57,1 kJ
|
Πηγές: |